Nonostante la disponbilità e l'uso diffuso dei vaccini contro il virus dell'influenza (IAV), la malattia continua ad avere un impatto importante per la suinicoltura. I vaccini utilizzati nei suini normalmente sono realizzati con virus interi inattivati (WIV-whole inactivated virus) che contengono un adiuvante del tipo olio in acqua e che si somminitrano per via intramuscolare. Sono stati sviluppati altri sistemi e negli USA esiste un vaccino di subunità che contiene una particella del RNA non replicante di alfavirus che codifica il gene HA. Inoltre, gli allevamenti possono sviluppare i propri vaccini stabulogeni. Normalmente, la vaccinazione viene fatta nelle scrofe per generare anticorpi materni che saranno trasferiti alle figliate via colostro, tuttavia, a volte, si usa vaccinare anche i suini da macello. Pur essendoci vari vaccini completamenti registrati, questi non si aggiornano con la stessa velocità con i virus cambiano antigenicamente. Questo può causare una protezione subottimale contro ceppi antigenicamente differenti.
Per la registrazione di un vaccino, dobbiamo dimostrare che questo è sicuro ed efficace. Per soddisfare i requisiti di efficacia, i fabbricanti devono dimostrare l'immunogenicità della formulazione mediante l'inibizione dell'emoagglutinazione (HI-hemagglutination inhibition) e/o riduzione dei titoli viremici a livello polmonare di suini vaccinati e sottoposti a challenge con ceppo omologo al virus vaccinale. Il tempo richiesto per modificare la formulazione di un vaccino che è già registrato secondo la legislazione americana è particorlamente lungo e dipende da ogni paese, questo ostacola gli aggiornamenti che sarebbero necessari per adattare il vaccino alla rapida evoluzione del virus. Tuttavia, recenti cambi della legislazione americana portati a termine dal Centro di Biologia Veterinaria dell'USDA (USA) potrebbero ridurre questo tempo in futuro.

In un contesto di campo, l'efficacia vaccinale dipende da ogni allevamento che è unico e da quello che si desidera ottenere. Il test di HI, lo standard delle proprietà antigeniche, normalmente sono correlati con i titoli della neutralizzazione virale che si utilizza per conferire protezione. Normalmente, si considera che un titolo di 40 o superiore è protettivo, tuttavia, i titoli sierici di HI non sempre sono ben correlati con l'efficacia e la protezione vaccinale; in alcuni casi anche contro gli stessi ceppi se alcuni fattori interferiscono nel momento in cui si somministra il vaccino.
Raggiungere l'autorizzazione di un vaccino è un processo laborioso, caro e che può essere considerevolmente lungo. Idealmente, gli aggiornamenti nella formulazione dei vaccini per suini nei confronti dell'IAV potrebbero seguire un processo similare a quello che si conduce con la selezione dei ceppi per adattare i vaccini nell'uomo alla stagionalità annuale, basandosi sulla vigilanza ed identificazione nazionale o regionale di nuovi ceppi antigenicamente differenti (figura 1). La sfida che si radica nell'evoluzione genetica ed antigenica del virus dell'influenza suina è molto più dinamica di quella dei virus umani, con una variazione sostanziale tra diverse regioni geografiche, inclusa la cocircolazione di molti ceppi distinti in una stessa regione(Vincent et al., 2014).
L'adozione di decisioni sui vaccini si basa sulla vigilanza e sul monitoraggio dei ceppi circolanti di IAV (figura 1). I primi passi per sviluppare un programma di selezione di vaccini più dinamici ed aggiornati sono l'analizzare le sequenze disponibili dei virus dei suini circolanti e le posizioni antigeniche conosciute nella sequenza aminoacidica dell'HA. Disgraziatamente, la similitudine della sequenza degli aminoacidi (e, in minor misura, la similitudine dei nucleotidi) non sempre è indicativa di protezione crociata. Nei virus suini H3, le grandi variazioni antigeniche si producono in 6 posizioni di aminoacidi vicino al recettore di HA e inclusa la sostituzione di un solo aminoacido ha un impatto significativo sulla antigenicità (Lewis et al., 2014). Al contrario, i virus suini H1, hanno una diversità genetica più complessa, probabilmente come risultato di una loro evoluzione a partire da virus classici e dalla ripetuta introduzione di virus umani nei suini durante un lungo periodo di tempo. Come conseguenza le variazioni antigenetiche non sono state attribuite a mutazioni di un unico aminoacido all'interno delle emoagglutinine H1, anche se la sostituzione di un unico aminoacido in, o vicino, al recettore ha un importante effetto accumulativo sull'antigenicità. Pertanto, la caratterizzazione antigenica è un passo cruciale che deve essere utilizzata in combinazione con la sequenziazione e le informazioni epidemiologiche per avere maggiori informazioni nell'adozione delle decisioni (figura 1).
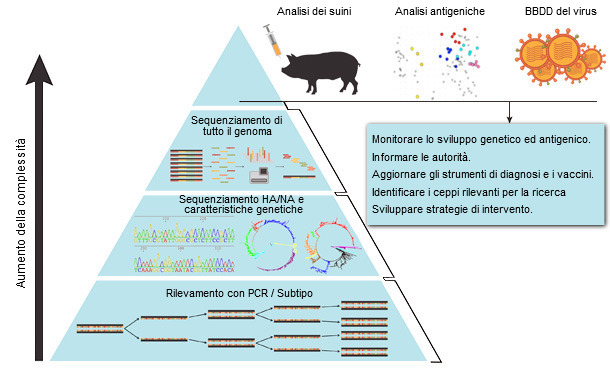
Figura 1. Metodo sistematico di vigilanza del virus dell'influenza A nel suino (basato su Ampofo et al., 2015).
In condizioni di circostanze ideali, la risposta immunitaria generata con vaccini inattivati è sufficiente per ridurre i segni clinici ed i titoli virali nei polmoni dopo l'infezione, sempre che questa sia prodotta da un virus molto similare antigenicamente. Tuttavia, i vaccini inattivati spesso non bloccano completamente l'infezione nelle condizioni di campo normali. Gli anticorpi materni generati a partire dalla vaccinazione delle scrofe possono proteggere i suinetti contro i segni clinici, però non contro l'infezione, e possono essere rilevati fino a 14 settimane d'età (Loeffen et al., 2003). Un effetto negativo di questi anticorpi è che possono interferire con l'efficacia vaccinale e con la risposta immunitaria attiva dei suinetti vaccinati. Di fatto l'immunità precedente, che sia passiva o acquisita, può interferire con la risposta immunitaria nei confronti dei vaccini morti.
E' improbabile che gli anticorpi stimolati da vaccini inattivati o da quelli acquisiti per trasferimento passivo possano fornire una protezione crociata completa contro l'infezione da un virus diverso, il che porta ad un fallimento vaccinale e maggiori costi per i suinicoltori. Il fallimento vaccinale può complicarsi tuttavia di più se la vaccinazione induce anticorpi di reazione crociata nei confronti di un HA dello stesso subtipo che impedisce la neutralizzazione in una infezione successiva (ovvero, senza reattività crociata nel test HI) il che può finire che produce la malattia respiratoria aggravata associata al vaccino(VAERD-vaccine-associated enhanced respiratory disease;(Gauger et al., 2011)). Affinchè si produca la VAERD, è necessario che gli HA e NA tra il virus del vaccino e quello infettivo non coincidano. E' stato dimostrato che il VAERD esiste in molti scenari sperimentali e ci sono indizi che si produca sul campo.
Le limitazioni dei vaccini inattivati ad indurre protezione crociata contro virus antigenicamente diversi, evidenziano la necessità di sviluppare vaccini che abbiano una protezione crociata più ampia. Sono stati usati vari sistemi vaccinali nei confronti dell'IAV dei suini e tutti hanno i loro pro e contro (figura 2). I vaccini vivi attenuati IAV (LAIV) hanno dimostrato di essere sicuri in condizioni sperimentali e più efficaci contro virus antigenicamente differenti (figura 2), riducendo la trasmissione virale e superando l'interferenza degli anticorpi materni (Pena et al., 2011; Vincent et al., 2012). I vaccini a subunità e i vaccini ad RNA o DNA basati sull' HA e NA si sono dimostrati ugualmente capaci di proteggere contro l'infezione, con il vantaggio tecnologico di essere semplici le modificazioni delle formulazioni dei vaccini per poter essere aggiornato ad altri antigeni provenienti dalla comparsa di nuovi virus (Wesley et al., 2004). Si continuerà a ricercare nuovi sistemi vaccinali come alternativa ai vaccini inattivati.
 Inattivato |
 |
 Attenuati |
|
| Via di somministrazione | intramuscolare | intramuscolare/intranasale | intranasale |
| Risposta HI | +++ | ++ | + |
| Cellule secernenti anticorpi | ++ | + | + |
| Cellule B memoria | + | + | + |
| IgA nasale | -/+ | -/+ | +++ |
| Anticorpo NA | +++ | -/+ | ++ |
| Cellule CD4 T | ++ | ++ | +++ |
| Cellule CD8 T | - | + | + |
| Immunità crociata | -/+ | + | ++ |
| Malattia respiratoria aggravata associata alla vaccinazione (VAERD) | yes | -/+ | no |
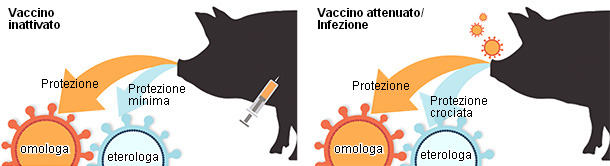
Figura 2. Efficacia comparativa tra diverse piattaforme vaccinali nei confronti dell'infezione da virus dell'influenza A nei suini
(basato su Sridhar et al., 2015).
La strategia vaccinale deve essere pianificata per ogni caso specifico, secondo le circonstanze. I vaccini inattivati possono essere efficaci se si utilizzano in combinazione con altre pratiche, come per esempio lo spostamento controllato di animali e persone e con un'analisi dettagliata per quanto riguarda l'antigene vaccinale, verificando la coincidenza con quello del ceppo in circolazione. E' necessario sapere quali ceppi sono in circolazione in ogni allevamento. L'Influenza Suina è una malattia dinamica che si modifica continuamente, per cui le strategie di monitoraggio e controllo devono essere accurate e dinamiche.




